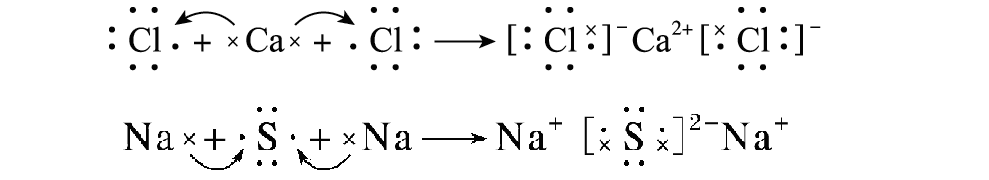一百多种元素的原子构成的物质种类已经超过一亿种,原子之间是通过一定的相互作用形成各种各样的物质的。
把相邻的原子之间存在的强烈相互作用叫化学键。原子在形成物质时一般要形成8个电子(K层2个电子)的稳定结构,这样符合能量最低原理。
一、离子键
从原子结构的角度分析钠原子和氯原子形成氯化钠的过程。
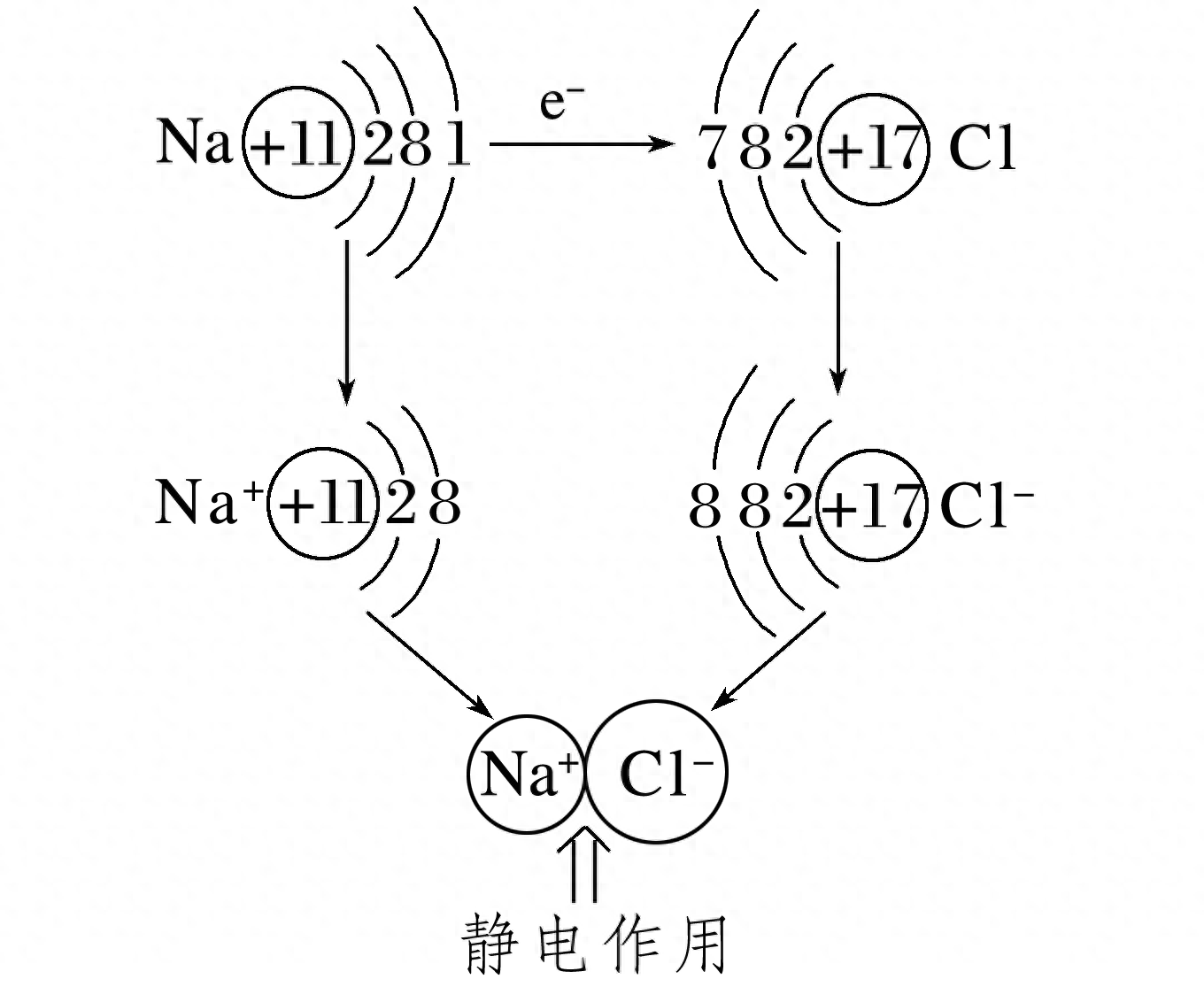
钠原子的最外层只有一个电子,容易失去一个电子形成8个电子的稳定结构,成为带一个单位正电荷的钠离子;氯原子的最外层有7个电子,容易得到一个电子形成8个电子的稳定结构,成为带一个单位负电荷的氯离子。
Na+和Cl-通过静电作用(包括静电引力和静电斥力)结合在一起,形成NaCl。Na+和Cl-之间的静电作用是一种强烈的相互作用,叫离子键。可见离子键本质上就是一种静电作用。
上述过程也可用电子式表示:

NaCl这种由离子键形成的化合物叫离子化合物,离子键一般由活泼的金属与活泼的非金属形成。
小结:
离子键的概念。

离子键
注意:金属与非金属形成的化学键不一定是离子键,如Al和Cl元素形成的是共价键,不是离子键,AlCl3是共价化合物不是离子化合物。
离子化合物:由离子键构成的化合物。

离子化合物
注意:铵盐是离子化合物。还有一些特别的离子化合物,如NaH、Mg3N2等。离子化合物中一定含有离子键,含离子键的化合物一定是离子化合物。
离子键、离子化合物及形成过程可用电子式表示:
在元素符号周围用“·”或“×”来表示原子的最外层电子。如:
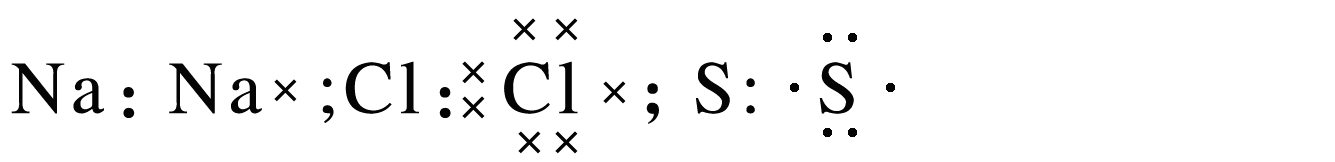
单核阳离子电子式与离子符号相同,原子团形成的阳离子要画出最外层电子,并用中括号写上所带的电荷数。如:

阴离子的电子式要画出最外层电子,并用中括号写上所带的电荷数。如:

离子化合物的电子式由阳离子和阴离子构成:如:
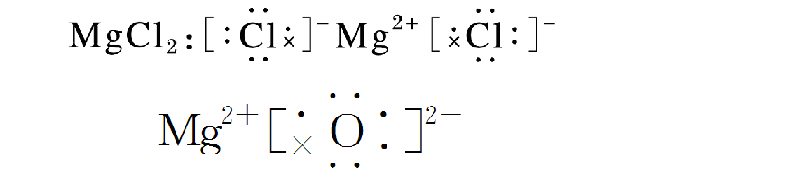
还可以用电子式表示离子键和离子化合物的形成过程。如: